ملزمة وحدة طبيعة المادة ومكوناتها علوم المستوى الثامن
الوحدة الأولى :
_ طبيعة المادة و مكوناتها :
1 - ما هي الذرات ؟
- أصغر جسيم لعنصر ما
2 - هل تتكون ذرات العنصر من نوع واحد أو أكثر من الذرات ؟
- ذرات العنصر تكون من نوع واحد و تختلف عن ذرات العناصر الأخرى
_ مثال :
- الألومنيوم عنصر ، إذا تابعنا قصه إلى نصفين متساوين ، يفترض أن نصل إلى جسيم واحد و هو الذرة
3 - كم عدد الذرات التي توجد في الطبيعة و هل يمكن صنع بعضها بالمختبر ؟
- يوجد 92 عنصراً تم العثور عليها في الطبيعة ، و 26 عنصراً تم صنعها في التجارب المختبرية ، و لكل منه نوع مختلف من الذرات
4 - اذكر بعض الأمثلة على العناصر :
الليثيوم / المغنيسيوم / الكربيتون / النحاس / النيتروجين / الكلور / الذهب / الصوديوم / الأكسجين / الألومنيوم / الحديد .
5 - أكمل الفراغ في السؤال التالي :
أ - أصغر جزء من المادة و لا يسهل تجزئته يسمى ( الذرة )
ب - يتكون من مجموعة من الذرات المتشابهة من نفس النوع هو ( العنصر )
6 - أجب عن السؤال التالي :
_ لماذا تختلف العناصر عن بعضها ؟
- لاحظ الصور لثلاثة عناصر و هي غاز الكلور و فلز الذهب و عنصر الكربون لاحظ الفرق بين ذرتها

_ إذا لماذا تختلف العناصر عن بعضها ؟
- تختلف العناصر عن بعضها بسبب اختلاف ذراتها
توالت أبحاث العلماء لمعرفة تركيب الذرة و قدم العلماء نماذج مختلفة عن الذرة و منهم :
دالتون - طومسون - رذرفورد - نماذجهم ؟
- أولا : نموذج دالتون
المادة تتكون من جسيمات صغيرة منفردة أطلق عليها اسم الذرات مثل دالتون هذه الذرات على شكل مجسما كروية صلبة لذلك سميت نموذج دالتون

- ثانيا : نموذج طومسون :
( ) أن الذرة جسيم كروي مصمت موجب الشحنة به جسيمات تحمل شحنة سالبة سميت الإلكترونات
( ) أن الشحنة الموجبة للذرة تساوي مجموع الشحنات السالبة للإلكترونات
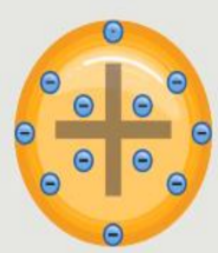
1 - أجب عن السؤال التالي :
أ - ضع عنوانا للشكل ، و حدد أسماء الجسيمات السالبة و الجسيمات الموجبة ، و أكتبها على الشكل .

- ثالثا : نموذج رذرفورد
قام العالم رذرفورد بتجربته الشهيرة حول الذرة عام 1911 م حيث قام بتسليط نوع من الأشعة موجبة الشحنة ( جسيمات ألفا ) على صفيحة رقيقة من الذهب
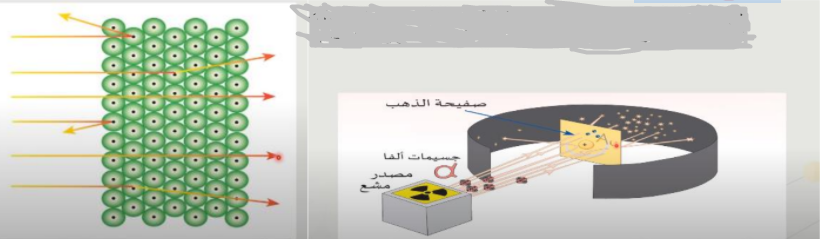
1 - ملاحظاته و استنتاجاته بناء على التجربة كانت كما يلي :
_ ملاحظات رذرفورد استنتاجات رذرفورد
معظم جسيمات ألفا نفذت دون انحراف ------> معظم حجم الذرة فراغ
نسبة قليلة من جسيمات ألفا ارتدت للخلف ------> تتركز كتلة الذرة في النواة
نسبة قليلة من جسيمات ألفة انحرفت عن مسارها ------> شحنة نواة الذرة موجبة ( تتنافر مع جسيمات ألفا )
2 - ما الجسيم الذي اكتشه العالم جيمس تشادويك ؟
النيوترونات
رابعا : نموذج بور :
نموذج بور : كيف تترتب الإلكترونات حول النواة ؟
في أغلفة أو مستويات طاقة
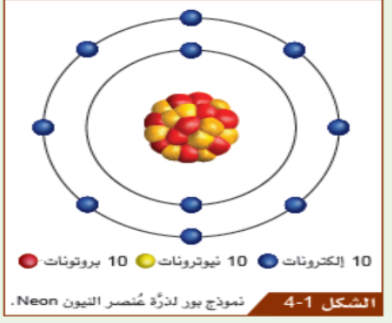
1 - مم تتكون الذرات ؟
تتكون من جسيمات صغيرة تسمى البروتونات + و النيوترونات و الإلكترونات
الذرات جميعها تمتلك نواة تحتوي في داخلها على البروتونات و النيوترونات إضافة إلى إلكترونات تدور في إفلاك حول النواة
2 - بما تمتاز ذرة الهيدروجين عن غيرها من الذرات ؟
ذرات الهيدروجين تحتوي على بروتون واحد فقط أي بدون نيوترون
3 - أجب عن الأسئلة التالية :
_ ما عدد البروتونات الموجبة في الشكل المجاور ؟
6 بروتونات
4 - ما عدد الإلكترونات السالبة في الشكل المجاور ؟
6 إلكترونات
5 - فكر ماذا تعني هذه العبارة “ الذرة متعادلة كهربيا " ؟
الذرة متعادلة كهربيا لأن عدد الشحنات الموجبة ( البروتونات ) يساوي عدد الشحنات السالبة ( الالكترونات ) و في هذه الذرة عدد البروتونات الموجبة = عدد الإلكترونات السالبة = 6
6 - انظر للصورة ثم قارن بين الجسيمات الثلاث في الجدول الآتي :
| وجه المقارنة | البروتونات | الالكترونات | النيوترونات |
| شحنة الجسيم | موجبة | سالبة | متعادلة |
| عدد الجسيمات | 3 | 3 | 4 |
تمتلك الأنواع المختلفة من الذرات أعداد مختلفة من البروتونات و النيوترونات و الإلكترونات ، فذرات النحاس مثلاً تمتلك بروتونات و إلكترونات أكثر مما تمتلكه ذرات الكبريت
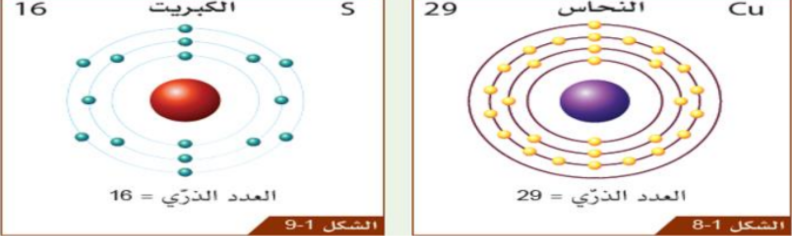
العدد الذري :
هو عدد البروتونات الموجودة في ذرة واحدة من ذرات العنصر
النشاط 1 : كيف تحسب عدد الجسيمات في الذرة ؟
1 - استخدم العدد الذري لحساب عدد البروتونات و الإلكترونات في ذرة العنصر ، أكمل الجدول التالي :
| العنصر | العدد الذري | عدد البروتونات | عدد الالكترونات |
| الألومنيوم | 13 | ||
| الكلور | 17 | ||
| الحديد | 26 | ||
| الذهب | 79 |
2 - اكمل الجدول التالي :
| العنصر | الرمز الكيميائي | عدد البروتونات | عدد النيوترونات | عدد الإلكترونات | العدد الذري |
| الفلور | F | 9 | 10 | 9 | |
| السيليكون | Si | 14 | 14 | 14 | |
| التيانيوم | Ti | 22 | 26 | 22 |
كلا من البروتونات و النيوترونات و الإلكترونات جسيمات منتاهية في الصغر لذلك اصطلح العلماء على الإشارة لكتلتها بوحجة تسمى وحدة الكتل الذرية أو amu
البروتون = 1 وحدة كتل ذرية
النيوترون = 1 وحدة كتل ذرية
الإلكترون = 840 1 / 1 وحدة كتل ذرية
بما أن البروتونات و النيوترونات موجودة داخل النواة و ذات كتل متساوية ، و الإلكترونات في مدارات حول النواة إلا أنها أصغر بكثير من كتلة البروتون الواحد لذا فإن معظم كتلة الذرة تتركز في النواة
علما بأن العدد الذري لعنصر الأكسجين = 8 و لعنصر الكبريت = 16 أي مما يأتي يمثل العبارى الصحيحة ؟
أ - تمتلك ذرة الأكسجين ضعف عدد البروتونات التي تمتلكها ذرة الكبريت
ب - تمتلك ذرة الكبريت 16 بروتون أكثر مما تمتلكه ذرة التي تمتلكها ذرة الأكسجين
جـ - تمتلك ذرة الكبريت ضع عدد البروتونات التي تمتلكها ذرة الأكسجين
د - تمتلك ذرة الأكسجين ضعف عدد الإلكترونات التي تمتلكها ذرة الكبريت
_ كيف تتم تسمية العناصر ؟
1 - أجب عن الأسئلة التالية :
أ - ما المشترك بين عناصر كل مجموعة ؟
كلها يشار إليها برموز من حروف لاتينية ( حرف أو حرفين )
بالرغم من اشتراك عناصر المجموعة الواحدة في الحرف الأول إلا أنها تختلف في الحرف الثاني و بعضها يشار إليه بحرف وحيد ، فسر ذلك ؟
للتميز بين العناصر التي تبدا بنفس الحرف