تدريبات منتصف الفصل الأول كيمياء المستوى الحادي عشر علمي الفصل الأول نقدمها لكم بأسلوب سهل وممتع للقارئ و المتعلم
1 - أي مما يلي صحيح عن خصائص الجسيمات المكونة للذرة ؟
A - البروتونات والإلكترونات لهما نفس الكتلة ونفس نوع الشحنة .
B - البروتونات والنيترونات لهما نفس الشحنة ويختلفان في الكتلة .
C - البروتونات والإلكترونات لهما نفس نوع الشحنة ولكنهما يختلفان في قيمة الشحنة
D - البروتونات والإلكترونات لهما نفس قيمة الشحنة ولكنهما يختلفان في نوع الشحنة
2 - ما السبب في أن الشحنة الكهربائية لا تظهر على الذرة ( الذرة متعادلة كهربائياً ) ؟
A - الشحنة الموجبة لكل بروتون تلغي الشحنة السالبة لكل الكترون
B - الشحنة الموجبة لكل بروتون تلغي الشحنة المتعادلة لكل نيترون
C - الشحنة السالبة للبروتون تلغي الشحنة الموجبة للإلكترون
D - الشحنة الموجبة للنيترون تلغى الشحنة السالبة للبروتون
3 - ذرة الكلور تحتوي على 17 بروتون و18 نيترون , أي مما يلي صحيح عن ذرة الكلور ؟
A - العدد الذري 18 ويحدد الخواص الكيميائية للذرة
B - العدد الذري 18 ويحدد الخواص الفيزيائية للذرة
C - العدد الذري 17 ويحدد الخواص الفيزيائية للذرة
D - العدد الذري 17 ويحدد الخواص الكيميائية للذرة
4 - أي مما يلي غير صحيح عن وصف التركيب الذري ؟
A - تتركز كتلة الذرة في النواة
B - تحدد الإلكترونات جميع الخواص الكيميائية للعنصر
C - أعداد البروتونات والنيترونات متساوية في الذرة المتعادلة كهربائية
D - ذرات العنصر نفسه يمكن ان تحتوي على اعداد مختلفة من النيترونات.
5 - أي مما يلي غير صحيح عن القوى الكهربية الساكنة؟
A - تؤدي إلى تماسك الذرة وثباتها
B - تعتبر سبباً لكل تفاعل كيميائي
C - تفسر كيفية تكون الروابط الكيميائية بين الذرات
D - الشحنات الكهربية المتعاكسة تتنافر والشحنات الكهربية المتشابهة تتجاذب.
7 - كم عدد الأفلاك الموجودة لعدد الكم الثانوي 3=l ؟
7A
5B
3C
1D
8 - ما هي اعداد الكم الأربعة (s,m,l,n) لإلكترون موجود في المستوى الرئيسي الثالث والمستوى الفرعي p داخل الفلك ( px) ويتحرك عكس اتجاه عقارب الساعة ؟

11 - كم عدد الأفلاك الموجودة في المستوى الفرعي f ؟
14A
7B
3C
6D
12 - كم عدد الإلكترونات الموجودة في المستوى الفرعي p ؟
14A
10B
6C
2D
13 - كم عدد الإلكترونات الموجودة في المستوى الرئيسي 4 = n؟
32A
16B
8C
2D
14 - كم عدد الأفلاك الموجودة في المستوى الرئيسي 2=n؟
32A
16B
8C
2D
15 - ما عدد الكم الذي يختلف فيه الإلكترونان الموجودان في نفس الفلك ؟
A - عدد الكم الرئيسي.
B - عدد الكم الثانوي.
C - عدد الكم المغزلي.
D - عدد الكم المغناطيسي
أجب عن الأسئلة التالية :
1 - بم تفسر :
- الذرة متعادلة كهربيا .( لا تظهر شحنة كهربية على الذرة) :
.................................................................................................................................................................................................. .................................................................................................................................................................................................
- أهمية القوى الكهروستاتيكية للذرة:
.................................................................................................................................................................................................. .................................................................................................................................................................................................. .................................................................................................................................................................................
- الكترونات الفلك الواحد لا تتنافر :
.................................................................................................................................................................................................. ..................................................................................................................................................................................................
- يتسع المستوى الفرعي P لست الكترونات فقط :
.................................................................................................................................................................................................. .................................................................................................................................................................................................
ما القيم الممكنة لعدد الكم المغناطيسي للمستوى الفرعي d ؟
.................................................................................................................................................................................................. .................................................................................................................................................................................................. .................................................................................................................................................................................................
- أكتب نص نموذج نظرية بور :
.................................................................................................................................................................................................. .................................................................................................................................................................................................. .................................................................................................................................................................................................. .......................................................................................................................................................................................
س2 : أكمل الجدول الآتي :
عدد الكم | أهميته |
عدد الكم الثانوي |
|
عدد الكم المغناطيسي |
|
عدد الكم الرئيسي |
|
عدد الكم المغزلي |
|
1 - أي مما يلي صحيح عن التوزيع الإلكتروني الآتي :
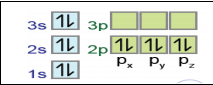
A - العنصر الفلزي وله تكافؤ يساوي 6
B - العنصر الفلزي وتكافؤه يساوي 2
C - العنصر فلزي وتكافؤه يساوي 2
D - العنصر فلزي وتكافؤه يساوي 6
4 - أي مما يلي ينتهي بالتوزيع الألكتروني الآتي 5 3P ؟
Na A
Mg B
P C
Al D
أجب عن الأسئلة الآتية :
س1 : ما عدد الكترونات التكافؤ للتوزيع المقابل ؟
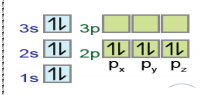
| المستوى الفرعي | S | P | D | F |
| عدد الأفلاك | ||||
| عدد الالكترونات | ||||
| عدد الكم الثانوي | ||||
| عدد الكم المغناطيسي | ||||
| الشكل |
س 3: رتب المستويات الفرعية تصاعدياً حسب الطاقة :
س 4 : أكمل الجدول الآتي :
| العنصر | التوزيع الالكتروني | مخطط الأفلاك ( طريقة هوند ) | التركيب النقطي |
| Na11 | |||
| 3 -N | |||
| 3+Al | |||
| Cr24 | |||
| Cu29 |
السؤال الأول : أكمل الجدول الآتي :
| الجزيء | CO | +H3O | + NH4 |
| تركيب لويس | |||
| الذرة المانحة | |||
| الذرة المستقبلة |
السؤال الثاني : ارسم التمثيل النقطي ( تركيب لويس ) لكل من :
| C2H4 | C2H2 | C2H5OH |
السؤال الثالث : عرف الرابطة الفلزية ؟
.................................................................................................................................... ...................................................................................................................................
السؤال الرابع : ما العلاقة بين عدد الكترونات التكافؤ والرابطة الفلزية و درجة الانصهار والصلابة ؟
..................................................................................................................................... ...................................................................................................................................
السؤال الخامس : رتب العناصر الآتية تصاعدياً حسب درجة الانصهار مع ذكر السبب ؟
Be , Li , B
السؤال الأول : رتب العناصر الآتية حسب القوة في السلبية الكهربية؟
Li - K - Na Cs
الأقل …………………………………………………… الأعلى
1 - ما الشكل الهندسي لجزيء تساهمي يحيط بالذرة المركزية 4 مناطق سالبة ( كثافة الكترونية ) اثنان منها تكون روابط ؟
A - هرم رباعي الوجوه
B - مثلث هرمي
C - خطي
D - غير خطي
2 - ما الشكل الهندسي لجزيء تساهمي يحيط بالذرة المركزية 3 مناطق سالبة( كثافة الكترونية ؟
A- هرم رباعي الأوجه
B - مثلث هرمي
C - مثلث مسطح
D - خطي
3 - أي مما يأتي صحيح عن المركب H2O ؟
| الشكل الهندسي | قيمة الزاوية | الأزواج الحرة | |
| A | غير خطي | 104.5 | لا يوجد |
| B | مثلث مسطح | 120 | يوجد |
| C | خطي | 180 | لا يوجد |
| D | غير خطي | 104.5 | يوجد |
4 - ما الشكل الهندسي لجزيء تساهمي يحيط بالذرة المركزية 4 مناطق سالبة ؟
A - هرم رباعي الأوجه
B - غير خطي
C - مثلث هرمي
D - خطي
1 : أكتب التوزيع الالكتروني لذرة الكربون في الحالة الاعتيادية والحالة المثارة والحالة المهجنة :
أ - ذرة الكربون في الحالة العادية
ب - ذرة الكربون في الحالة المثارة
1 - ذرة الكربون المهجنة ( SP3 )
2 - ذرة الكربون المهجنة ( SP2 )
3 - ذرة الكربون المهجنة ( SP )
السؤال الثاني :أكمل الجدول الاتي :
| CH4 | C2H4 | C2H2 | |
| نوع التهجين | |||
| عدد المناطق السالبة | |||
| الشكل الهندسي | |||
| الزاوية | |||
| عدد الروابط سيجما | |||
| عدد الروابط باي |
السؤال الثالث :أكمل الجدول الاتي :
| الجزيء | تركيب لويس | الأزواج الحرة | الأزواج المرتبطة | الشكل الهندسي | الزاوية | نوع التهجين | القطبية |
| BeCl2 | |||||||
| AlBr3 | |||||||
| CH4 | |||||||
| NF3 | |||||||
| H2S |
السؤال الرابع : أكمل الجدول الاتي :
| الجزيء | H2O | PH3 |
| تركيب لويس | ||
| الأزواج الحرة | ||
| الأزواج المرتبطة | ||
| الشكل الهندسي | ||
| الزاوية مع التفسير | ||
| التهجين | ||
| القطبية |
السؤال الأول : اختر الإجابة الصحيحة :
1 - ما المصطلح العلمي الذي يعبر عن ( قوى جذب ضعيفة تنشأ بواسطة قوى ثنائية قطب لحظية )
A - قوى ثنائي القطب
B - قوى لندن التشتتية
C - الرابطة الهيدروجينية
D - الرابطة الفلزية
2 - أي مما يلي صحيح عن الهالوجينات ؟
A - اليود غاز بسبب زيادة الكتلة الجزيئية ونقص قوى لندن التشتتية
B - الكلور سائل بسبب نقص الكتلة الجزيئية ونقص قوى لندن التشتتية
C - البروم سائل بسبب زيادة الكتلة الجزيئية وزيادة قوى لندن التشتتية
D - الفلور غاز بسبب زيادة الكتلة الجزيئية وزيادة قوى لندن التشتتية
السؤال الثاني:
1 - عدد التطبيقات الحياتية للرابطة الهيدروجينية ؟
.........................................................................................................................................................................................................
.........................................................................................................................................................................................................
.........................................................................................................................................................................................................
.........................................................................................................................................................................................................
.....................................................................................................................................................................................................
2 - فسر ما يلي :
أ - الكلور غاز بينما اليود صلب :
ب - درجة غليان HF أعلى من HCl
ج - درجة غليان الأرجون أعلى من درجة غليان الهيليوم .
د - درجة غليان الماء HO2 أعلى من الميثان CH4 .